Swiss Health Web
EMH Schweizerischer Ärzteverlag AG
Farnsburgerstrasse 8
CH-4132 Muttenz
+41 (0)61 467 85 44
support@swisshealthweb.ch
www.swisshealtweb.ch
Publiziert am 02.02.2021
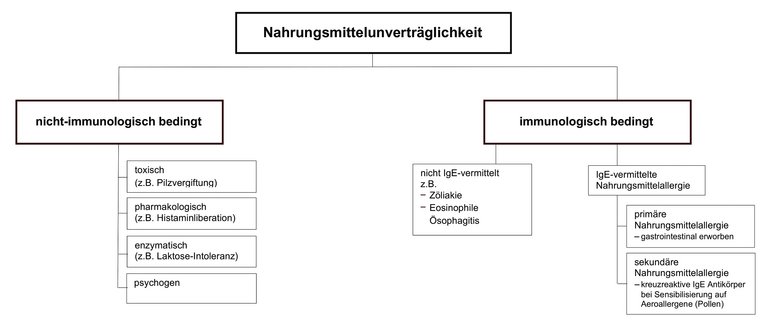
Nahrungsmittelallergien (NMA) sind relativ häufige Feststellungen im Praxisalltag. Es gilt zwischen primären und sekundären NMA zu unterscheiden.
| Tabelle 1: Überblick klinisch relevanter pflanzlicher Allergene. Bei den pflanzlichen Allergenen sind vier verschiedene Proteinfamilien klinisch relevant. Das Risiko schwerer Reaktionen nimmt zu: Profiline → PR-10 Proteine → LTP → Speicherproteine. | |||
| Profiline | PR-10 Proteine (Pathogenesis related protein 10) Bet v1-homologe | LTP (Lipid Transfer Proteine) | Speicherproteine |
| Hitze- und Protease-sensible Proteine | Hitze- und Protease-sensible Proteine | Hitze- und Protease-resistente Proteine | Hitze- und Protease-resistente Proteine |
| Sensibilisierung inhalativ (Pollen) | Sensibilisierung inhalativ (Pollen) | Sensibilisierung evtl. via GI-Trakt | Sensibilisierung in der Regel via Gastrointestinaltrakt |
| Symptome: OAS Bei Co-Sensibilisierung mit Bet v1 nicht als relevant beurteilt | Symptome: OAS, selten ASR | Symptome: oft ASR, v.a. mengenabhängig. Vorkommen: Mittelmeerländer auch ohne Birkensensibilisierung | Symptome: meist ASR |
| Leitallergene: Bet v2 (Birke), Phl p12 (Wiesenlischgras) | Leitallergen: Bet v1 (Birke) | Leitallergen: Pru p3 (Pfirsich) | Leitallergene: Ara h2 (Erdnuss), Jug r1 (Walnuss) |
| Abkürzungen: ASR = allgemein systemische Reaktion; OAS = orales Kontaktallergiesyndrom. | |||
| Tabelle 2: Beispiele ausgewählter pflanzlicher Nahrungsmittelallergen-Komponenten. | ||||
| Profiline | PR-10 Proteine | Lipid Transfer Proteine | Speicherproteine | Identifizierte Allergene |
| Cor a2 | Cor a1 | Cor a8 | Cor a9, 11, 14 | Haselnuss |
| Mal d4 | Mal d1 | Mal d3 | Apfel | |
| Gly m3 | Gly m4 | Gly m5,6 | Soja | |
| Pru p4 | Pru p1 | Pru p3 | Pfirsich | |
| Ara h5 | Ara h8 | Ara h9 | Ara h1-4, 6,7 | Erdnuss |
| Tabelle 3: Wichtigste Auslöser primärer Nahrungsmittelallergien bei Kindern und Erwachsenen. |
| Kuhmilch |
| Hühnerei |
| Weizen |
| Soja |
| Erdnuss |
| Schalenfrüchte (Nüsse) |
| Fisch |
| Meeresfrüchte |

| Tabelle 4: Liste kennzeichnungspflichtiger Nahrungsmittelallergene [8]. | |
| 1. | Glutenhaltiges Getreide, namentlich Weizen, Roggen, Gerste, Hafer, Dinkel, Kamut oder Hybridstämme davon, sowie daraus hergestellte Erzeugnisse |
| 2. | Krebstiere und daraus gewonnene Erzeugnisse |
| 3. | Eier und daraus gewonnene Erzeugnisse |
| 4. | Fische und daraus gewonnene Erzeugnisse |
| 5. | Erdnüsse und daraus gewonnene Erzeugnisse |
| 6. | Sojabohnen und daraus gewonnene Erzeugnisse |
| 7. | Milch und daraus gewonnene Erzeugnisse (einschliesslich Laktose) |
| 8. | Schalenfrüchte, namentlich Mandeln (Amygdalus communis L.), Haselnüsse (Corylus avellana), Walnüsse (Juglans regia), Cashewnüsse (Anacardium occidentale), Pecannüsse (Carya illinoinensis), Paranüsse (Bertholletia excelsa), Pistazien (Pistacia vera), Macadamia- oder Queenslandnüsse (Macadamia ternifolia) sowie daraus gewonnene Erzeugnisse |
| 9. | Sellerie und daraus gewonnene Erzeugnisse |
| 10. | Senf und daraus gewonnene Erzeugnisse |
| 11. | Sesamsamen und daraus gewonnene Erzeugnisse |
| 12. | Schwefeldioxid und Sulfite (ab 10 mg/kg bzw. 10 mg/l) |
| 13. | Lupinen und daraus gewonnene Erzeugnisse |
| 14. | Weichtiere und daraus gewonnene Erzeugnisse |
| Tabelle 5: Notfallmedikamente zur Abgabe an den Patienten. | |
| Erwachsene | |
| Antihistaminika | z.B. 2×5 mg Levocetirizin, 2×10 mg Cetirizin |
| Corticosteroide | 2×50 mg Prednisolon |
| Adrenalin-Autoinjektor* | 0,3 mg i.m (EpiPen®/Jext®) |
| Kinder | |
| Antihistaminika | z.B. Cetirizin Tropfen 0,25 – 0,5 mg/kgKG, Levocetirizin Tropfen 0,125 – 0,25 mg/kgKG |
| Corticosteroide | 2 mg Prednisolon/kgKG alternativ Betnesol, auflösbare Tabletten 0,3 mg/kgKg |
| Adrenalin-Autoinjektor * | 7,5 kgKG–25 kgKG: 0,15 mg, ab 25 kgKG 0,3 mg |
| * Ein Adrenalin-Autoinjektor sollte dann abgegeben werden, wenn es sich um eine primäre Nahrungsmittelallergie handelt oder der Patient schwer reagiert hat. Die Entscheidung, ob ein Adrenalin-Autoinjektor indiziert ist oder nicht, fällt nicht immer leicht, im Zweifelsfall sollte ein Adrenalin-Autoinjektor abgegeben werden und anschliessend eine Abklärung durch den Allergologen erfolgen. | |
Veröffentlicht unter der Copyright-Lizenz.
"Attribution - Non-Commercial - NoDerivatives 4.0"
Keine kommerzielle Weiterverwendung ohne Genehmigung.
See: emh.ch/en/emh/rights-and-licences/